Причины мужского бесплодия: режим дефицита, лептин, инсулин
Экология жизни. Здоровье: В последнее время мы наблюдаем рост частоты бесплодия. Ранее я говорил о том, как проблемы с лептином и инсулинорезистентность связаны с женским бесплодием, теперь поговорим о мужском. Напомню, что репродуктивная сфера – одна из самых энергоемких, поэтому при режиме дефицита страдает одна из первых.
В последнее время мы наблюдаем рост частоты бесплодия. Ранее я говорил о том, как проблемы с лептином и инсулинорезистентность связаны с женским бесплодием, теперь поговорим о мужском. Напомню, что репродуктивная сфера – одна из самых энергоемких, поэтому при режиме дефицита страдает одна из первых.
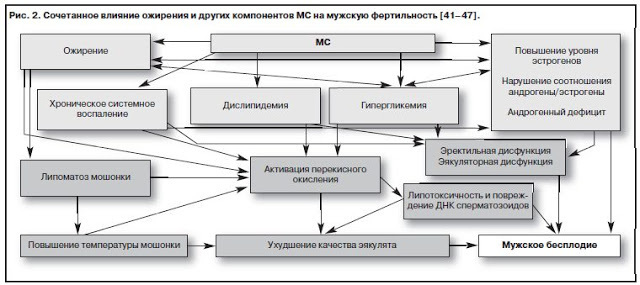
Впрочем, снижение либидо и плодовитости в условиях режима дефицита – это естественная защитная биологическая реакция. Вернемся к мужскому бесплодию и метаболическому синдрому (режиму дефицита). Клиническая значимость ожирения у мужчин значительно выше, чем у женщин: оно гораздо труднее поддается лечению традиционными методами, ведет к ускорению развития и прогрессирования сердечно-сосудистых заболеваний, приводя к уменьшению средней продолжительности жизни у мужчин по сравнению с женщинами на 8–12 лет. Механизмы негативного влияния избыточной массы тела и ожирения на мужскую репродукцию достаточно разнообразны.
Бесплодие – это неспособность соматически здоровой семейной пары репродуктивного возраста, не применяющей средства контрацепции, достичь зачатия в течение 12 месяцев регулярной половой жизни. Частота бесплодных браков в мире катастрофически растет: в Европе и США она составляет 15%, в Канаде – 17%, а в России приближается к 20%. В последнее время мужское бесплодие сравнялось по частоте с женским – частота «мужского» фактора в семейном бесплодии достигает 40-50%.
Причины мужского бесплодия: лептин
При ожирении наблюдается повышение уровня лептина в крови (маркер объема жировой ткани и активности адипоцитов), что получило название «лептинорезистентность», при этом лептин индуцирует клинический андрогенный дефицит за счет снижения чувствительности андрогеновых рецепторов к тестостерону и блокады синтеза лютеинизирующего гормона в гипофизе, с одной стороны, и усиления ароматизации тестостерона на периферии в эстрадиол под влиянием ароматазы жировой ткани – с другой.
Синергизм эффектов обоих патологических процессов ведет к глубоким нарушениям репродуктивной системы мужчин с ожирением, связанных не только с окислительным стрессом на фоне избытка свободных жирных кислот и триглицеридов в крови, но и за счет дефицита тестостерона – ключевого полового стероида, необходимого для нормального сперматогенеза.
D.Goulis и B.Tarlatzis (2008 г.) считают, что ожирение приводит к уменьшению уровня общего тестостерона и глобулина, связывающего половые стероиды, которое становится проявлением негативного влияния жировой ткани на тестикулярную функцию. Хотя точные патофизиологические механизмы такого взаимодействия остаются неясными, предполагается, что лептин, резистин и грелин (гормоны жировой ткани) играют важную роль во взаимодействии между ожирением и тестикулярной дисфункцией.
С другой стороны, возникающий при ожирении андрогенный дефицит усугубляет инсулинорезистентность, которая является главным, наряду с ожирением, патофизиологическим механизмом, запускающим системный оксидативный стресс, ведущий к патозооспермии. P.Mah и G.Wittert (2010 г.) приводят аналогичные данные о том, что ожирение у мужчин достоверно ассоциируется с низким уровнем общего и свободного тестостерона крови, которые, в свою очередь, повышают риск развития ИР и СД типа 2.
Гипогонадизм у мужчин с ожирением может быть также следствием системного хронического воспаления, которое закономерно развивается на фоне ожирения, и часто сопутствующего ожирению дефицита гормона D, крайне необходимого для синтеза тестостерона и поддержания репродуктивной функции у мужчин. При ожирении в клетках Лейдига наблюдается нарушение цепи трансформации холестерина под влиянием цитохрома Р450 за счет способности ФНО-a и ИЛ-1 ингибировать стероидогенез, что ведет к уменьшению синтеза тестостерона.
Нарушения синтеза тестостерона при ожирении у мужчин составляют сегодня «эндокринологическую аксиому» андрологии, так как, с одной стороны, несмотря на то что тестостерон не является непосредственным индуктором сперматогенеза, он абсолютно необходим для его поддержания, с другой стороны, патогенетическая связь андрогенного дефицита и ожирения у мужчин сегодня достоверно доказана.
Это чрезвычайно важно для понимания патофизиологических системных эффектов ожирения, которые в настоящее время описываются термином «липотоксичность жировой ткани» и которые принимают самое активное участие в индукции и прогрессировании системного оксидативного стресса с негативным влиянием на сперматогенную и стероидогенную функции.
Избыток свободных жирных кислот и триглицеридов в крови при ожирении обусловливает запуск системного окислительного стресса, который приводит к избыточному накоплению свободных радикалов в клетках и тканях разных органов, включая скелетные мышцы, миоциты сердца, гепатоциты, b-клетки поджелудочной железы, ренальный и тестикулярный эпителий, что приводит к хронической дисфункции клеток вследствие их повреждения. Триглицериды обладают токсичностью, обусловленной неэстерифицированными жирными кислотами с длинной цепью и их продуктами (керамиды и диацилглицеролы).
Индуцированная неэстерифицированными жирными кислотами с длинной цепью митохондриальная дисфункция тестикулярного эпителия является основным механизмом нарушений структуры и функции яичек у мужчин при ожирении, а одновременное уменьшение содержания антиоксидантов в системном кровотоке усугубляет дальнейшее прогрессирование оксидативного стресса и способствует ему.
Рост бесплодия в индустриально развитых странах связывают с воздействием на репродуктивную систему целого ряда неблагоприятных медикосоциальных, алиментарных и психологических факторов, ведущих к повышению общей заболеваемости современной популяции, среди которых в настоящее время бесспорным лидером является ожирение, часто приводящее к сахарному диабету 2 типа (СД 2 типа) и андрогенному дефициту у мужчин и, как следствие, существенно повышающее риск развития у них оксидативного (и воспалительного) спермального стресса.
В рутинной андрологической практике не существует стандартных рекомендаций по скрининг-диагностике оксидативного стресса сперматозоидов у бесплодных мужчин, но совершенно очевидно, что чем раньше выявлен и скорректирован оксидативный стресс сперматозоидов, тем меньшие репродуктивные потери несет мужчина.
Причины мужского бесплодия: воспалительно-оксидативный стресс
При этом крайне важно иметь в виду, что оксидативный стресс сперматозоидов достоверно присутствует не только у мужчин с урологической патологией (например, при варикоцеле или воспалительных заболеваниях предстательной железы), но и практически всегда имеет место при ожирении, сахарном диабете или андрогенном дефиците, независимо от наличия или отсутствия у бесплодного мужчины патологии репродуктивной системы.
Ожирение является доказанным системным фактором, негативно влияющим на мужскую репродукцию посредством ранней инициации системного оксидативного стресса, приводящего при избыточном накоплении свободных радикалов кислорода в эякуляте к фрагментации ДНК сперматозоидов (спермальному оксидативному стрессу). Менее известен урологам-андрологам метаболический феномен инсулинорезистентности (ИР), который закономерно рано или поздно развивается при прогрессировании ожирения и который характеризуется нарушением чувствительности тканей к глюкозе, что приводит к митохондриальной недостаточности сперматозоидов (все тот же спермальный оксидативный стресс).
И если сегодня уже многие врачи связывают репродуктивные потери с ожирением и рекомендуют своим бесплодным пациентам с избыточной массой тела снизить ее, то ранняя диагностика и коррекция ИР пока не стала нормой обследования каждого бесплодного мужчины с ожирением, хотя именно ИР является той самой ранней (доклинической) и потому обратимой стадией сахарного диабета 2 типа, которую можно и нужно активно выявлять у всех мужчин с бесплодием на фоне ожирения. ИР приводит к гликолизному стрессу нервных окончаний, т.е., по сути, инициирует метаболическую урогенитальную нейропатию, приводящую к нарушению эякулятодинамики и фертильных свойств эякулята.
Причины и механизм развития бесплодия
Снижение уровня тестостерона (андрогенный дефицит) все чаще сегодня рассматривается как возможно новый и патогенетически важный компонент МС у мужчин, так как доказано, что частота и выраженность андрогенного дефицита у мужчин находится в достоверной обратной связи не только с частотой и выраженностью ожирения, но и инсулинорезистентности и сахарного диабета 2 типа.
Не только ожирение (ИМТ >30), но даже просто избыток веса (индекс массы тела ИМТ=25-29) у мужчин достоверно повышают частоту бесплодия по сравнению с мужчинами, имеющими нормальный индекс массы тела (ИМТ=20-22,4). Ожирение ухудшает качество эякулята за счет уменьшения его объема и повышению частоты повреждения ДНК сперматозоидов. Сахарный диабет 2 типа – частый спутник ожирения – может приводить к развитию эякуляторной дисфункции, что также может вызывать нарушение доставки сперматозоидов в половые пути женщины.
В последнее время окислительная теория патогенеза мужского бесплодия становится очень популярной, при этом метаболический синдром в ней играет одну из главных ролей. Компоненты МС приводят к увеличению свободных радикалов активного кислорода в эякуляте с последующей гиперпероксидацией мембран сперматозоидов и повреждением их ДНК.
Таким образом, наличие МС у мужчины любого возраста с бесплодием является показанием не только для уточнения причин гормональнометаболических нарушений, но и активного поиска оксидативного стресса сперматозоидов
Современные литературные источники связывают снижение репродуктивного потенциала у мужчин с ожирением с такими патофизиологическими феноменами, как дефицит половых гормонов (прежде всего тестостерона), гормона D, эндотелиальная дисфункция и дефицит регионарного кровообращения, в том числе тестикулярного кровотока, на фоне выраженной вазоконстрикции вследствие развивающегося при гипогонадизме дефицита оксида азота (NO); избыточная активность прооксидантной системы крови; избыток триглицеридов и свободных жирных кислот, которые в конечном итоге, действуя синергически, приводят к тяжелому системному окислительному стрессу, вызывающему окислительный стресс сперматозоидов с повреждением и дестабилизацией мембран и митохондрий сперматозоидов, нарушением упаковки и целостности ДНК в хромосомах половых клеток, инициацией апоптоза сперматозоидов, что закономерно заканчивается нарушениями морфологии и подвижности половых клеток, снижением их количества и оплодотворяющей способности.
Согласно общепринятой точке зрения оксидативный стресс сперматозоидов развивается при нарушении динамического равновесия между окислителями и антиоксидантами в семенной плазме, а его частота при мужском бесплодии, по данным разных авторов, достигает 30–80%. Гиперпродукция активных форм кислорода – свободных радикалов – может быть обнаружена при многих патологических состояниях, как связанных с репродуктивной системой (местные факторы – воспаление половых придаточных желез, варикоцеле, урогенитальные инфекции), так и не связанных с ней непосредственно, которые играют роль системных механизмов оксидативного стресса сперматозоидов (любой психоэмоциональный стресс, СД типа 2): ожирении, системном хроническом воспалении, курении, плохой экологии, особенностях образа жизни и питания .
Таким образом, в настоящее время объяснение влияния многих негативных патофизиологических механизмов ожирения (системного хронического воспаления, дислипидемии, нарушений углеводного обмена, андрогенного дефицита, жировой липотоксичности и др.) на сперматогенез прямо или косвенно ассоциируется с теорией оксидативного стресса сперматозоидов, который они индуцируют в течение всего времени, пока у мужчины имеется ожирение, персистенции и развитию которого они способствуют при прогрессировании ожирения у бесплодного мужчины.
Причины мужского бесполодия: инсулинорезистентность
Инсулинорезистентность, или гиперинсулинемия, являясь ключевым патогенетическим фактором МС, есть комплекс компенсаторно-приспособительных реакций, развивающихся на фоне ожирения, часто ассоциированного с андрогенным дефицитом у мужчин.
При развитии и прогрессировании ожирения резко снижается экспрессия гена рецептора инсулина, что ведет к уменьшению плотности рецепторов на поверхности клеток и возникновению резистентности к инсулину, а одновременное повышение уровня основного гормона жировой ткани – лептина – разрушает функциональную связь между гипофизом и гонадами, что является патогенетической основой формирования и прогрессирования андрогенного дефицита у мужчин одновременно с прогрессированием ожирения и ИР.
Развивающаяся ИР сопровождается гиперинсулинемией, которая в данном случае обеспечивает поддержание эффективности углеводного обмена, жизнеспособности и деления клеток. ИР – самая ранняя и поэтому потенциально обратимая стадия СД 2 типа, поэтому ее раннее выявление при любых соматических заболеваниях у мужчин с ожирением является важной профилактической мерой в отношении СД 2 типа и андрогенного дефицита.
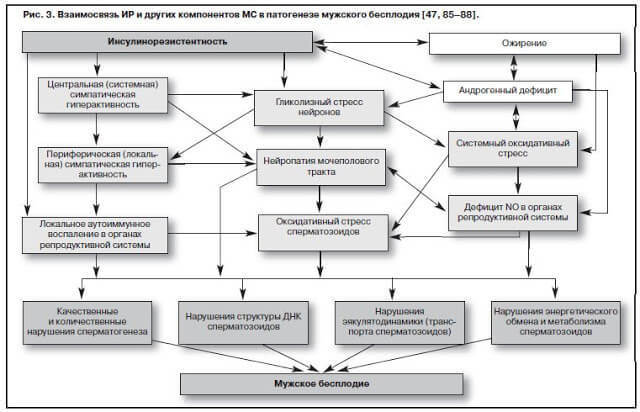
Ранняя диагностика ИР показана всем мужчинам репродуктивного возраста с ожирением и любыми другими компонентами МС, так как мужское бесплодие (особенно так называемое идиопатическое) может быть патогенетически связано с ИР, механизмы которой в данном случае могут сводиться к следующим:
Раннее нарушение структуры и функции нервной ткани (гликолизный стресс), при этом первоначальные повреждения отмечаются в самых мелких периферических нервных окончаниях органов урогенитальной системы (почки, половой член, предстательная железа, яички) (эффект индукции и прогрессирования урогенитальной метаболической нейропатии).
Нейропатия ведет к системным и местным реакциям вазоконстрикторного типа и заканчивается развитием эндотелиальной дисфункции вследствие дефицита основного вазодилататора – оксида азота NO (т.к. 90% синтеза оксида азота происходит не в эндотелии, а в терминалях нервных окончаний сосудов).
Любая нейропатия ассоциируется с активацией системы перекисного окисления липидов – системным оксидативным стрессом, который является мощным повреждающим фактором для паренхимы яичек, что заканчивается нарушениями сперматогенеза (бесплодием) и (или) стероидогенеза (андрогенным дефицитом). Вариантом данного системного эффекта ИР является окислительный (оксидативный) стресс сперматозоидов.
ИР и ожирение, являясь ключевыми компонентами МС, инициируют системное хроническое воспаление (цитокиновые каскадные реакции), которые активно участвуют в реализации еще одного механизма повреждающего действия на ткань яичек (аналога окислительного стресса) – ренальной липотоксичности, приводящей к нарушению структуры ДНК сперматозоидов.
Кроме того, гиперинсулинемия ведет к повышению системной симпатической активности через нарушение метаболизма глюкозы в вентромедиальных гипоталамических нейронах, что сопровождается повышенной активностью a-адренорецепторов урогенитального тракта (автономной симпатической гиперактивностью, или нейропатией) и запускает системный окислительный стресс. M.Sankhla и соавт. (2012 г.) при обследовании 120 мужчин в возрасте 17–26 лет с ожирением и бесплодием выявили достоверное повышение уровня малонового диальдегида (маркера системного окислительного стресса) с увеличением ИМТ (р<0 div="" nbsp="">
Среди механизмов нарушения фертильности у больных с нарушениями углеводного обмена некоторые авторы называют характерное для этой группы пациентов поражение придатков яичек, что способно привести к нарушениям транспорта сперматозоидов, а также урогенитальную нейропатию (гликолизный стресс нейронов), оксидативный стресс, приводящий к повреждению ядерной и митохондриальной ДНК сперматозоидов и их повышенной иммобилизации, а также дефицит NO вследствие андрогенной недостаточности и нейропатии, так как 90% NO, синтезируемого в сосудистой стенке, имеет нейрональное происхождение.
Заключение
Таким образом, у бесплодных молодых мужчин с ожирением при отсутствии у лечащего врача настороженности всегда имеется опасность гиподиагностики ключевого компонента МС – ИР, которая оказывает существенное негативное влияние на сперматогенез. С этой точки зрения, нам представляется, что частота идиопатического бесплодия за счет раннего выявления ИР могла бы оказаться ниже, чем об этом принято говорить. Идиопатическое бесплодие сегодня – это чаще всего бесплодие без явной урологической причины, так как проблемы репродукции у нас в стране традиционно отнесены к компетенции урологов. .
Это настоятельные требования XXI века – века патогенетической и профилактической медицины и междисциплинарных взаимодействий. Поэтому современный уролог из хирурга должен превращаться в клинициста и активно взаимодействовать со смежными специалистами (эндокринологами, терапевтами, неврологами).
Это Вам будет интересно:
Меридиональное простукивание: техника эмоциональной свободы
Ключ к мышцам кора: поясничная мышца (psoas)
Если этого не произойдет, то имеется большая вероятность того, что при решении мужских репродуктивных проблем в нашей стране уролог скоро будет простым диспетчером, который выписывает семейной паре исключительно направления в клиники репродукции, поскольку мы не в состоянии остановить мировую эпидемию «болезней цивилизации», которые сегодня являются ведущими системными патофизиологическими инициаторами оксидативного стресса сперматозоидов, клинически заканчивающегося мужским бесплодием.опубликовано econet.ru
Автор: Андрей Беловешкин
Источник: https://econet.ru/
Понравилась статья? Напишите свое мнение в комментариях.
Ну и банально алкоголь, табак, стресс - все это тоже не на пользу сперматогенезу. Поэтому и советуют в период планирования собой заняться, вредные привычки устранить. Я спермактин форте принимал, сейчас жто лучший препарат для сперматогенеза, по дозировкам и эффективности лучше не найти
ОтветитьСпасибо. Очень важно, чтобы мужчина не боялся ходить к врачу, а то некоторые думают, если ничего не болит, то здоровье в норме. Мы с мужем лечились от бесплодия, анализы, узи, операция по удалению спаек… Муж СпермаПлант пил, в составе L-карнитин повышает оплодотворяющую способность спермы, кроме этого препарат снижает риск развития патологий плода. Хорошо, что все это закончилось, теперь в ожидании чуда)
ОтветитьДобавить комментарий