Электролиз: химики обнаружили, как производить лучшие электроды
Еще один шаг вперед в области возобновляемых источников энергии - производство зеленого водорода может стать еще более эффективным в будущем.
Применив необычную технологическую операцию, химики Университета Мартина Лютера Галле-Виттенберг (MLU) нашли способ обработки недорогих электродных материалов и значительного улучшения их свойств во время электролиза. Группа опубликовала результаты своих исследований в журнале ACS Catalysis.
Повышение эффективности производства зеленого водорода
Водород считается решением проблемы хранения возобновляемых источников энергии. Его можно производить в локальных электролизерах, временно хранить, а затем очень эффективно преобразовывать обратно в электричество в топливном элементе. Он также служит важным сырьем в химической промышленности.
Подписывайтесь на наш youtube канал!
Однако экологичному производству водорода по-прежнему препятствует слабая конверсия поставляемой электроэнергии. "Одна из причин этого заключается в том, что динамическая нагрузка колеблющегося электричества от солнца и ветра быстро вытесняет материалы до предела. Дешевые материалы катализатора быстро становятся менее активными", - говорит профессор Майкл Брон из Института химии MLU, объясняя основную проблему.
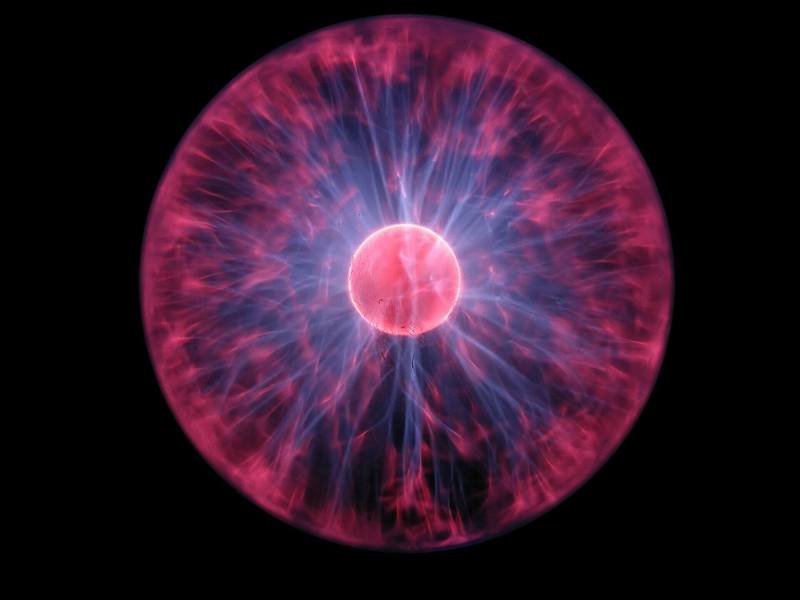
Электронные микрофотографии образцов NiO, обработанных при а) 300 °C, b) 500 °C,
c) 700 °C, d,e) 900 °C и f) 1000 °C, следует учитывать, что полоса белой шкалы составляет 50 нм для (а)-(е) и 200 нм для (f).
В настоящее время его исследовательская группа открыла метод, который значительно повышает как стабильность, так и активность недорогих никельгидроксидных электродов. Гидроксид никеля является дешевой альтернативой очень активным, но и дорогим катализаторам, таким как иридий и платина. В научной литературе рекомендуется нагревать гидроксид до 300 градусов. Это повышает стабильность материала и частично превращает его в оксид никеля. Более высокие температуры полностью разрушают гидроксид. "Мы хотели увидеть это собственными глазами и постепенно нагревали материал в лаборатории до 1000 градусов С", - говорит Брон.
По мере повышения температуры исследователи наблюдали ожидаемые изменения отдельных частиц под электронным микроскопом. Эти частицы превращались в оксид никеля, росли вместе, образуя более крупные структуры, и при очень высоких температурах образовывали узоры, напоминающие изображения зебры. Однако электрохимические испытания удивительным образом показали постоянно высокий уровень активности частиц, которые не должны были больше использоваться при электролизе. Как правило, при электролизе более активны большие поверхности и, следовательно, более мелкие структуры. "Поэтому мы связываем высокий уровень активности наших гораздо более крупных частиц с эффектом, который, как ни удивительно, происходит только при высоких температурах: образование активных оксидных дефектов на частицах", - говорит Брон.
Используя рентгеновскую кристаллографию, исследователи обнаружили, как при увеличении температуры изменяется кристаллическая структура гидроксидных частиц. Они пришли к выводу, что при нагревании до 900 градусов С - точки, в которой частицы проявляют наибольшую активность, - дефекты проходят переходный процесс, который завершается при 1000 градусах С. В этой точке активность снова внезапно падает.
Брон и его команда уверены, что нашли многообещающий подход, так как даже после повторных измерений после 6000 циклов нагретые частицы все еще вырабатывают на 50% больше электричества, чем необработанные частицы. Далее исследователи хотят использовать рентгеновскую дифракцию, чтобы лучше понять, почему эти дефекты так увеличивают активность. Они также ищут способы получения нового материала, чтобы более мелкие структуры сохранялись даже после термической обработки. опубликовано econet.ru по материалам techxplore.com
Подписывайтесь на наш канал Яндекс Дзен!
P.S. И помните, всего лишь изменяя свое потребление - мы вместе изменяем мир! © econet
Источник: https://econet.ru/
Понравилась статья? Напишите свое мнение в комментариях.
Добавить комментарий